Al via ai test per il Molnupiravir: si attende esito Ema

L’Ema ha avviato una revisione continua per Molnupiravir, la cosiddetta “pillola Merck”, un farmaco antivirale orale sperimentale per il trattamento di Covid-19 negli adulti, sviluppato dalla società Agenzia farmaceutica Msd, di cui la Redazione Notix ha parlato qualche giorno fa. In una nota l’Agenzia Europea del Farmaco ha confermato che se sarà concessa l’autorizzazione all’immissione in commercio dalla Commissione europea, il Molnupiravir potrebbe essere la prima pillola antivirale per il trattamento del Covid-19 nell’Unione europea.
“Sebbene” l’Ema “non possa prevedere le tempistiche complessive, dovrebbe essere necessario meno tempo del normale per valutare un’eventuale autorizzazione all’immissione in commercio, a causa del lavoro svolto durante la rolling review”, conclude la nota.
Potrebbe interessarvi...

Salute, Ema approva estensione del vaccino per i bambini tra i 5 e 11 anni
Salute, Ema approva estensione del vaccino per i bambini tra i 5 e 11 anni

Caccia al super farmaco: 700 dollari a trattamento per la “pillola Merck”
"La pillola della Merck" è la nuova versione del vaccino che promette a chi si è infettato di combattere i
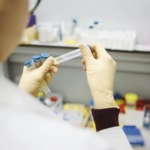
L’Ema valuta nuovo farmaco anti-Covid
La revisione proseguirà finché non vi saranno evidenze sufficienti per consentire all'azienda di presentare una richiesta formale di autorizzazione
L’Ema valuta nuovo farmaco anti-Covid
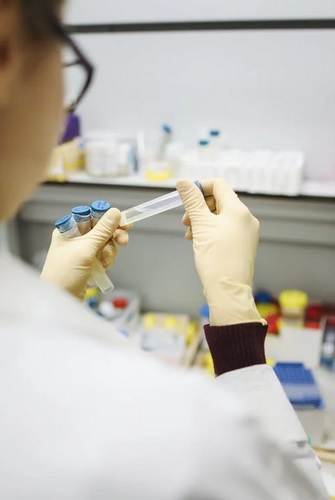
L’Agenzia europea dei medicinali ha avviato una revisione continua del trattamento Evusheld, una combinazione di due anticorpi monoclonali sviluppata da AstraZeneca per la prevenzione del Covid-19 negli adulti. La decisione “si basa sui risultati preliminari di studi clinici, che suggeriscono che il medicinale può aiutare a proteggere dalla malattia”, rende noto Ema.
La decisione del Chmp si basa sui risultati preliminari di studi clinici – ricorda l’Ema – che suggeriscono la capacità del farmaco di proteggere dalla malattia causata dal coronavirus Sars-CoV-2. L’agenzia Ue – si legge in una nota – ha iniziato a esaminare i dati preclinici (ottenuti da studi di laboratorio e su animali), e analizzerà più informazioni relative a qualità, sicurezza ed efficacia del trattamento non appena saranno disponibili. La revisione proseguirà finché non vi saranno evidenze sufficienti per consentire all’azienda di presentare una richiesta formale di autorizzazione all’immissione in commercio.
Potrebbe interessarvi...

Campania, il bollettino covid di sabato 14 maggio
Nelle ultime 24 ore sono stati effettuati 18.892 antigenici e 7.190 molecolari per un totale di 26.082 tamponi. Il controllo

Campania, il bollettino covid di venerdì 13 maggio
Nelle ultime 24 ore sono stati effettuati 15.788 antigenici e 5.364 molecolari per un totale di 21.152 tamponi. Il controllo

Campania, il bollettino covid di giovedì 5 maggio
Nelle ultime 24 ore sono stati effettuati 19.846 antigenici e 7.165 molecolari per un totale di 27.011 tamponi. Il controllo
Da Ema attesa autorizzazione su monoclonali Ronapreve

“L’Agenzia europea per i medicinali (Ema) ha avviato la valutazione su una domanda di autorizzazione all’immissione in commercio per la combinazione di anticorpi monoclonali Ronapreve (casirivimab/imdevimab). Il richiedente è Roche Registration Gmbh”. Lo si apprende da una nota dell’Ema. Il farmaco Ronapreve, si legge, “è destinato al trattamento del Covid-19 negli adulti e negli adolescenti dai 12 anni di età che non richiedono ossigeno supplementare e che sono a maggior rischio di progressione alla forma grave” e, più in generale, “per la prevenzione del Covid-19 negli adulti e negli adolescenti dai 12 anni in su”.
“L’Ema valuterà i benefici e i rischi di Ronapreve in tempi ridotti e potrebbe emettere un parere entro due mesi”, precisa la nota.
Potrebbe interessarvi...

Salute, Ema approva estensione del vaccino per i bambini tra i 5 e 11 anni
Salute, Ema approva estensione del vaccino per i bambini tra i 5 e 11 anni

Al via ai test per il Molnupiravir: si attende esito Ema
In una nota l’Agenzia Europea del Farmaco ha confermato che se sarà concessa l'autorizzazione all'immissione in commercio dalla Commissione europea,

L’Ema valuta nuovo farmaco anti-Covid
La revisione proseguirà finché non vi saranno evidenze sufficienti per consentire all'azienda di presentare una richiesta formale di autorizzazione
Terza dose, arriva l’ok dall’Ema: “Fragili e over 18 almeno a 6 mesi da seconda”

Diversi Paesi, tra cui l’Italia, somministrano già la terza dose di vaccino anti-Covid ai soggetti più fragili. Oggi, l’Ema (Agenzia Europea del Farmaco) ha dato l’ok ai richiami “sui soggetti immunodepressi, almeno a 28 giorni di distanza dalla seconda dose”. L’Agenzia ha anche sottolineato che un richiamo con il vaccino Pfizer aumenta gli anticorpi nelle persone di età compresa tra i 18 e i 55 anni, se somministrato ad almeno 6 mesi di distanza dalla seconda dose. Ancora da valutare l’eventualità di un richiamo con il farmaco Spikevax, prodotto da Moderna.
Secondo l’Ema, le autorità sanitarie nazionali possono adottare raccomandazioni sull’utilizzo dei richiami tenendo conto dei dati finora acquisiti. “Il rischio di infiammazioni cardiache o altri effetti molto rari dopo un richiamo non è conosciuto – si legge in una nota – e viene attentamente monitorato. Come per tutti gli altri farmaci l’Ema continuerà a raccogliere e valutare tutti i dati sulla sicurezza e l’efficacia dei vaccini”. L’organizzazione delle campagne vaccinali nei vari Paesi Ue, resta “una prerogativa delle competenti autorità nazionali”.
Potrebbe interessarvi...

Salute, Ema approva estensione del vaccino per i bambini tra i 5 e 11 anni
Salute, Ema approva estensione del vaccino per i bambini tra i 5 e 11 anni

Al via ai test per il Molnupiravir: si attende esito Ema
In una nota l’Agenzia Europea del Farmaco ha confermato che se sarà concessa l'autorizzazione all'immissione in commercio dalla Commissione europea,

L’Ema valuta nuovo farmaco anti-Covid
La revisione proseguirà finché non vi saranno evidenze sufficienti per consentire all'azienda di presentare una richiesta formale di autorizzazione
Per Ema, possibile legame mRna con miocardite pericardite

Il Comitato per la farmacovigilanza dell’Ema ha concluso che la miocardite e la pericardite possono verificarsi in casi molto rari a seguito della vaccinazione con vaccini mRna di BionTech-Pfizer e Moderna. Il Comitato raccomanda pertanto di elencare la miocardite e la pericardite come nuovi effetti collaterali nelle informazioni sul prodotto per questi vaccini, insieme a un avvertimento per sensibilizzare gli operatori sanitari e le persone che assumono questi vaccini.
Potrebbe interessarvi...

Cultura: MiC, dal 1 aprile nuove regole per l’accesso a musei, mostre, archivi, biblioteche, cinema, teatri e concerti
Dal prossimo 1° aprile, con l’entrata in vigore del decreto-legge 24 marzo 2022, n.24, che stabilisce la fine dello Stato di
Cantieri della Cultura, MiC: 2,4 mln di euro per il Palazzo Baronale di Colonna
Il Ministero della Cultura ha stanziato un finanziamento di 2,4 milioni di euro per il restauro del Palazzo Baronale di

Salute, Ema approva estensione del vaccino per i bambini tra i 5 e 11 anni
Salute, Ema approva estensione del vaccino per i bambini tra i 5 e 11 anni
L’ Ema invita a monitorare tutte varianti: “Attenzione a Delta plus”

“Ci aspettiamo che emergano altre varianti, quindi è molto importante che si continui con il monitoraggio e la sorveglianza sull’efficacia dei vaccini” e oltre alla variante Delta ‘classica’ “è già emersa la Delta plus, che è la Delta con un’ulteriore mutazione nella proteina spike, che dobbiamo tenere sotto controllo”.
Potrebbe interessarvi...

Campania, il bollettino covid di sabato 14 maggio
Nelle ultime 24 ore sono stati effettuati 18.892 antigenici e 7.190 molecolari per un totale di 26.082 tamponi. Il controllo

Campania, il bollettino covid di venerdì 13 maggio
Nelle ultime 24 ore sono stati effettuati 15.788 antigenici e 5.364 molecolari per un totale di 21.152 tamponi. Il controllo

Campania, il bollettino covid di giovedì 5 maggio
Nelle ultime 24 ore sono stati effettuati 19.846 antigenici e 7.165 molecolari per un totale di 27.011 tamponi. Il controllo
Ema, venerdì il responso su Pfizer ai 12-15enni

L’Agenzia europea dei medicinali terrà una conferenza stampa venerdì alle 15 in cui riferirà delle sue conclusioni sull’autorizzazione del vaccino Comirnaty (Pfizer/BioNtech) ai 12-15enni.
Potrebbe interessarvi...

Il generale ucraino che scambia la propria vita per far evacuare i minori
Il generale Vyacheslav Abroskin si è proposto ai russi per poter portare i bambini fuori dalla città. Il vice capo

Alessandria, denunciati 7 minori per interruzione di pubblico servizio in concorso
La scorsa domenica, personale della Sezione Volanti della Questura di Alessandria deferiva all’Autorità Giudiziaria sette giovani per il reato di

Massa Carrara, servono alcolici ai minori: il Questore ammonisce due locali del centro cittadino
La Polizia di Stato, attraverso l’attivazione di una serie di servizi di prevenzione in orario diurno e serale, soprattutto nel
Ema estende “conservazione” Pfizer: e gli altri?
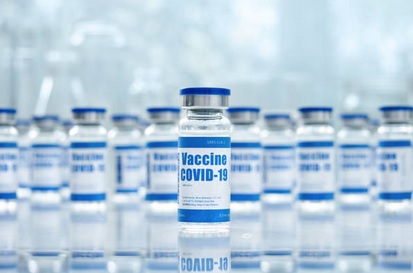
L’Agenzia europea del farmaco ha esteso da 5 giorni a un mese il periodo di conservazione approvato della fiala scongelata e non aperta del vaccino Pfizer/BioNtech a 2-8°C. “Si prevede che una maggiore flessibilità nella conservazione e nella manipolazione del vaccino avrà un impatto significativo sulla pianificazione e la logistica” del suo utilizzo negli Stati membri dell’Ue, spiega.
Potrebbe interessarvi...

Campania, il bollettino covid di sabato 14 maggio
Nelle ultime 24 ore sono stati effettuati 18.892 antigenici e 7.190 molecolari per un totale di 26.082 tamponi. Il controllo

Campania, il bollettino covid di venerdì 13 maggio
Nelle ultime 24 ore sono stati effettuati 15.788 antigenici e 5.364 molecolari per un totale di 21.152 tamponi. Il controllo

Campania, il bollettino covid di giovedì 5 maggio
Nelle ultime 24 ore sono stati effettuati 19.846 antigenici e 7.165 molecolari per un totale di 27.011 tamponi. Il controllo
Ema inizia review vaccino cinese Sinovac

Il Comitato per i medicinali umani (Chmp) dell’Ema ha avviato una rolling review, la revisione continua, del vaccino Covid-19 (Vero Cell), sviluppato da Sinovac Life Sciences.
Potrebbe interessarvi...

Somma Vesuviana, Spider-Man al centro vaccinale per i bambini
“Da pochi minuti si è concluso l’Open Day vaccinale a Somma Vesuviana per i bambini dai 5 agli 11 anni.

Salute, Ema approva estensione del vaccino per i bambini tra i 5 e 11 anni
Salute, Ema approva estensione del vaccino per i bambini tra i 5 e 11 anni

Campania, Ecco i dati dell’Unità di crisi. De Luca commenta
Campania, Ecco i dati dell'Unità di crisi. De Luca commenta
